Por Raquel Martín Baquero, alumna del Máster en Neurociencia de la UAM
Un modelo de depresión en ratones muestra que el tratamiento con una cepa bacteriana cuya presencia se encuentra disminuida en la microbiota intestinal de estos animales revierte los síntomas depresivos y aumenta la producción de nuevas neuronas en el cerebro. Esas son las conclusiones de un estudio llevado a cabo por investigadores del Instituto Pasteur de París, publicado recientemente en Nature Communications.
Además, en esta investigación, liderada por el profesor Pierre-Marie Lledo, experto en este tema, han encontrado que la alteración de la microbiota intestinal (la población bacteriana del intestino) modifica el metabolismo de las grasas, lo cual relacionaría el intestino y el cerebro. Estos hallazgos, muestran que una microbiota intestinal saludable contribuye a la función normal del cerebro
Los investigadores del Instituto Pasteur usaron un modelo de depresión en ratones. Trasplantaron heces desde estos ratones con depresión a ratones sanos y observaron que los animales sanos que recibieron el trasplante también presentaban síntomas depresivos, confirmando que existía una relación entre la población de bacterias intestinales y la depresión.
Como explica Pierre-Marie Lledo, Jefe de la Unidad de Percepción y Memoria del Institut Pasteur (CNRS / Institut Pasteur), que lidera el estudio: “Sorprendentemente, simplemente con transferir la microbiota de un animal con trastornos del estado de ánimo a un animal con buena salud es suficiente para provocar en él cambios bioquímicos y conferir comportamientos depresivos en estos últimos”.
Estudiaron si había alteraciones en la microbiota intestinal de estos ratones con depresión secuenciando su ADN y observaron modificaciones significativas en algunas familias bacterianas en comparación con la microbiota de ratones no enfermos.
Una de las familias de bacterias cuya presencia se encontraba reducida era la denominada Lactobacillaceae. En concreto, decidieron administrar la cepa bacteriana Lactobacillus plantarum, cuya función en la microbiota intestinal humana es regular el metabolismo de las grasas. Esta cepa bacteriana, presente en el yogur y otros derivados lácteo, tiene aplicaciones en el campo de los alimentos probióticos, ya que contribuye a estabilizar y normalizar la microbiota intestinal, al disminuir el pH por la producción de ácido láctico, que dificulta el crecimiento de microorganismos patógenos.
Recientemente se ha publicado un estudio en el cual L. plantarum aliviaba el estrés y la ansiedad en humanos. Por todo esto, administraron oralmente esta cepa bacteriana a los ratones con depresión cuya microbiota estaba alterada y observaron que los comportamientos depresivos se revertían y parcialmente se restauraba la producción de nuevas neuronas en el hipocampo de los ratones, estructura cerebral implicada en la formación de nuevas memorias y emociones.
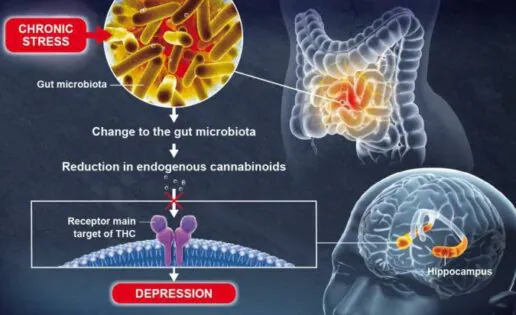
Buscando la relación entre las bacterias intestinales y el cerebro, estos investigadores encontraron que la microbiota de los ratones con síntomas depresivos altera el metabolismo de las grasas, lo cual lleva a una reducción en el hipocampo de unas moléculas denominadas endocannabinoides que coordinan un sistema de comunicación que regula las emociones y la respuesta al estrés.
Estos endocannabinoides se unen al mismo receptor que algunos derivados del cannabis, como el tetrahidrocannabinol (THC) que es su componente psicoactivo más importante y abundante y es, por lo tanto, responsable de los efectos del consumo recreativo de marihuana. Una reducción en los niveles de endocannabinoides en el hipocampo es suficiente para que aparezcan comportamientos depresivos y para que disminuya la producción de nuevas neuronas.
Además, el tratamiento con la bacteria Lactobacillus plantarum aumentaba los niveles de endocannabinoides en el cerebro, lo cual explicaría sus efectos antidepresivos.
Esta investigación propone que el sistema endocannabinoide sería la vía que relacionase las alteraciones en la microbiota con la depresión. Además, estos autores concluyen que el uso de bacterias específicas que se encuentran reducidas en el intestino podría resultar en un tratamiento muy prometedor para restaurar la microbiota y para tratar los trastornos depresivos.
La depresión es la principal causa de discapacidad en todo el mundo, afectando actualmente a más de 300 millones de personas. Es la enfermedad mental más prevalente en nuestro país (Haro et al., 2006). Según la última encuesta nacional de salud de 2017, un 6.68% de la población española habría recibido un diagnóstico de depresión por un médico en los últimos 12 meses. En total, aproximadamente tres millones de personas en nuestro país estarían diagnosticadas de esta enfermedad.
Te puede interesar
Salvador Martínez, ex director del Instituto de Neurociencias de Alicante, entrevista a Pierre-Marie Lledo (a la izquierda en el vídeo):
” La mayoría de nuestros metabolitos provienen de la microbiota intestinal, que debemos considerar como una empresa química en nuestro interior que produce compuestos que nosotros no somos capaces de sintetizar”
Otros temas







