Tanto el concepto de átomo como el de elemento tienen su origen en la Grecia clásica. Ya entonces algunos pensadores creían que la materia debía estar compuesta por partes pequeñas e indivisibles, los átomos, y por distintos tipos de ladrillos, ya que era evidente que el agua, la madera y el fuego, por ejemplo, tenían un comportamiento bien distinto. Por eso, algunos consideraban que había cuatro elementos: el aire, el fuego, el agua y la tierra.
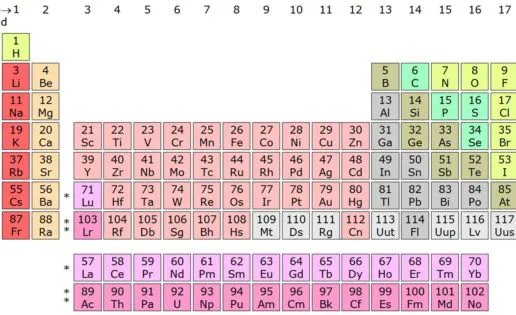
Esta idea sobrevivió en Occidente durante siglos y siglos. Los alquimistas empezaron a modificarla al comenzar sus estudios con los metales. Pero, con el florecimiento de la química sobre todo en el siglo XVIII, esta idea murió al fin: Lavoisier y otros introdujeron el concepto de elemento químico, como un material con unas propiedades características que se podían medir. De hecho, Mendeleiev, que no fue el primero en elaborar una tabla de elementos químicos, consiguió diseñar una clasificación en base a estas propiedades químicas y que permitía predecir cómo serían en base a ellas los elementos aún no descubiertos. A esta creación se la conoce como tabla periódica de los elementos, porque está construida en base a unas características que se repiten de forma cíclica (periódica).
Corría por entonces el año 1869 (la Guerra Civil americana había finalizado hacía unos cuatro años). En aquel momento, el trabajo meticuloso y constante de varias generaciones de químicos habían logrado descubrir 63 elementos químicos.
El 30 de diciembre de 2015 Mendeleiev estaba de nuevo de enhorabuena. La Unión Internacional de Química Pura y Aplicada anunciaba la incorporación de cuatro nuevos elementos químicos a la tabla periódica, con lo que el repertorio de elementos químicos conocidos alcanzaba la cifra de 118. Además, la séptima fila de la tabla quedaba completa y llegaba el momento de inaugurar una nueva fila para seguir descubriendo elementos. (Artículo sobre la incorporación de cuatro nuevos elementos y artículo sobre el japonio, el primer elemento descubierto en Asia).
Pero, ¿cómo son estos nuevos elementos? ¿Qué aspecto tienen y para qué sirven? Se lo pregunté a Bernardo Herradón, investigador científico del CSIC y miembro de la Real Sociedad Española de Química. Según explica, estos nuevos elementos no pueden encontrarse en la naturaleza ni tan siquiera pueden verse. Se han producido en laboratorio y se han obtenido en cantidades ínfimas, y su interés real es entender cómo funciona el interior de los átomos. De hecho, los científicos trabajan desde hace décadas en producir átomos cada vez más pesados a base de producir choques entre partículas: como resultado, el número de protones que albergan los núcleos se incrementa, y así es como se crean elementos químicos nuevos (el número de protones, también llamado Z, es la magnitud que define un elemento químico. Por ejemplo, el sodio se caracteriza por tener 11 protones en el núcleo y el oxígeno 8). Sin más, os dejo con él:

-¿Cuál es en su opinión la importancia de la incorporación de los nuevos cuatro elementos a la tabla periódica?
Es una investigación básica que prueba que es posible obtener núcleos de elementos superpesados haciendo colisiones entre núcleos de átomos menos pesados. De esta manera se prueban las predicciones teóricas que anticipan este comportamiento. Por otro lado, tener elementos químicos superpesados (con número atómico Z mayor de 100) es importante para conocer el balance de fuerzas (interacciones) que actúan en el núcleo de los átomos. en el caso del elemento 118, por ejemplo, hay 118 protones (con carga positiva) confinados en un espacio muy reducido. Desde el punto de vista electromagnético, las repulsiones harían imposible tener este núcleo; pero ahí actúa la interacción fuerte que mantiene los nucleones unidos.
-¿Tienen algo en común estos cuatro elementos? (Tengo entendido que son radiactivos, inestables, de vida media muy efímera…)
Sí, todos ellos son muy inestables, con existencias muy breves. De hecho, una parte muy importante de la investigación que ha conducido a los cuatro elementos es estudiar las rutas de desintegración de los mismos y, a partir de estos datos, confirmar la existencia de algunos isótopos de estos elementos. Nota: Los isótopos son átomos de un elemento (es decir que tienen el mismo número de protones), pero con un número distinto de neutrones.
-¿Por qué hay grandes laboratorios invirtiendo millones y millones en la síntesis de elementos cada vez más pesados? ¿Para qué lo hacen?
Actualmente son cinco: dos en USA (California y Tenessee), Rusia, Alemania y Japón. Es decir, paises influyentes que saben que invertir en ciencia básica es fundamental para el progreso de la nación. Como he mencionado antes, esta investigación es básica de la que no hay que esperar aplicaciones cotidianas inmediatas; pero estamos hablando de investigación en la frontera de la química, la física de partículas, física de altas energía, etc; todos estos campos tienen aplicaciones en nuestras vidas cotidianas: somos dependientes de la energía, por ejemplo.
La información científica que se obtiene de estos experimentos sirve para conocer detalles de los procesos de fusión nuclear, que pueden ser fundamentales para realizar en el futuro la fusión de los isótopos del hidrógeno (el proyecto ITER), lo que popularmente se ha llamado “el Sol en la Tierra”.
La investigación en aceleradores permite obtener elementos radiactivos que tienen aplicaciones en medicina nuclear, como el isótopo 99 del tecnecio, que se usa en el PET (tomografía de emisión de positrones). Y no hay que olvidar que la investigación con aceleradores de partículas del CERN fue el origen de INTERNET Sólo con este ejemplo, se justificaría la inversión en ciencia básica.
-Ahora que se ha completado el séptimo período, ¿qué vendría después? (¿Los superactínidos, quizás?)
Se ha previsto que a partir del elemento 120 se conseguirán núcleos más estables (y los de número atómico par más estabñe que los de nº atómico impar). Si se consiguen estos elementos lo mismo se puede estudiar sus propiedades físicas y químicas y se podrán confirmar ciertas propiedades que predecimos según la colocación de los elementos en el sistema periódico.
-¿Cuál es el elemento más pesado que hay en la naturaleza? ¿Por qué hay elementos entonces que se producen en laboratorio pero que no se encuentran fuera de ellos?
El elemento más pesado en nuestro planeta es el uranio (elemento Z = 92). De los elementos más ligeros que el uranio, el tecnecio (Z = 43) y el promecio (Z = 61) no se encuentran en nuestro planeta. Esto es porque son demasiado inestables y se desintegran en un tiempo relativamente corto comparado con la vida de nuestro planeta (alrededor de 4.500 millones de años). Los elementos transuránidos que se producen en el laboratorio son radiactivos y se desintegran en elementos más ligeros.
-¿Y dónde está el límite?
No hay límite. Lo que pasa es que cada vez es más difícil obtener elementos nuevos; pues para obtenerlos artificalmente es necesario hacer colisionar núcleos de elementos relativamente pesados, que deben ser acelerados hasta una velocidad muy alta y esto requiere mucha energía. Por eso, los elementos superpesados se obtienen con “cuentagotas”, aunque el hecho de que ahora se confirmen cuatro de ellos a la vez es anecdótico, pues las investigaciones se iniciaron hace unos 20 años en los cinco laboratorios mencionados (aunque uno de ellos, el alemán, no fue el primero)
-Tengo entendido que a los nuevos elementos que se descubren o proponen se les da nombres mitológicos, relacionados con minerales, lugares, países o científicos. ¿Hay alguna curiosidad que le haya llamado la atención en relación con estos nombres?
Para mí, la historia más curiosa es la del elemento Galio. Lo conté en un post hace un tiempo.
El enlace es http://www.madrimasd.org/blogs/quimicaysociedad/2011/11/23/132871
Échale un vistazo a ver si lo encuentras interesante.








